新版動物實驗計畫書(115版)申請&審查方式,與現行版本(113.2版)填寫對照表
新版動物實驗計畫書(115版)申請&審查方式(2026/2/1起適用),與現行版本(113.2版)填寫對照表
- 申請流程: 照目前的新案申請方式一樣,只是將新版動物實驗計畫書(115版)輸出成PDF檔案格式(word檔轉PDF檔),夾帶在補充說明文件#1位置(主管簽名頁另外上傳,見第4點)。
- 審查的版本: 只會針對115版動物實驗計畫書內容進行審理
- 審查流程(送件): 照原本的方式一樣。審查委員會將審查意見填入浮動視窗,申請人依照審查意見,在115版計畫內容進行修改(修改處粗體紅字標示),同時回覆系統上審查意見表委員提問。修改後的版本(複審),可再直接輸出成PDF檔案,替換原本#1位置的上一版計畫書。
- 審查流程主管簽名檔: 可以直接將該頁夾帶在原本「主管簽名檔」位置。列印那一頁進行簽核即可,不用再整份計畫書。
- 其餘補充說明文件: RG2同意書/人員教育訓練佐證文件/動物操作室規範申請書/動物實驗聲明書/動物實驗轉讓同意書,可夾帶在系統補充說明文件#2~之後的位置。
- 此階段申請方式為過渡時間,暫時由此方式進行申請,因動物實驗計畫是整個系統(包含訂購/代養/分籠離乳/PAM/監督報告/帳務計算)的源頭,所以源頭內的一些必填項目資訊(以下第8點),要麻煩各位研究人員配合填寫。未來新版系統完成後,將會依115版內容套用。
- 115版中的"試驗設計編號"地方包含第三大項、第七-1項、第十一項、第十二-2項、第十二-3項、第十四-1項等共六處,填寫時要注意一致性。
- 現行版本113.2版,以下是正確必填寫欄位(如計畫書115版有被委員要求修改,這些項次也要同步調整):
- 第一大項 基本資料
- 第二大項 實驗參與人員
- 第三大項 使用動物
- 第八-4-g項 儀器使用勾選
- 第九-6-a&b項 不利影響副作用&疼痛評估
- 第九-8-c 安樂死方法
- 上述現行版本(113.2版)如沒描述到的項目,可以參照以下對照表,將填寫好的新版計畫書內容,複製貼到相對應目前版本的位置,整理如下:
(記得將115版內容貼到113.2版系統相對應位置,以避免無法送出)
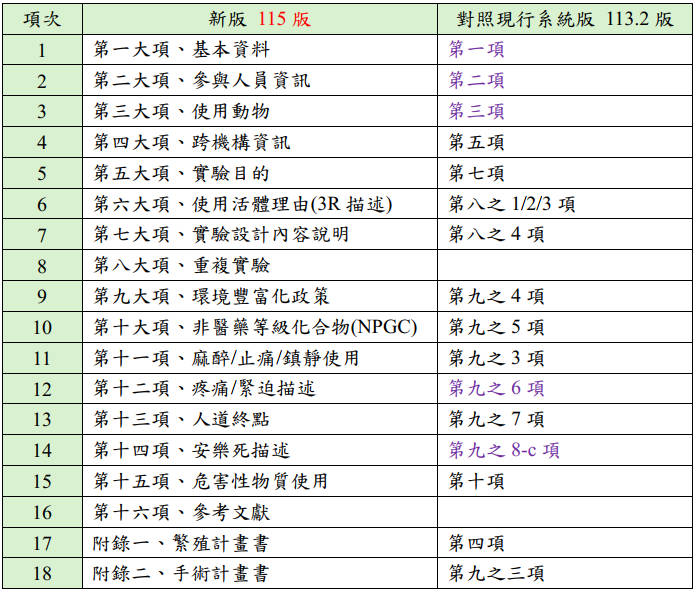
- 新版115版第一大項 基本資料對照系統版113.2版第一項
- 新版115版第二大項 參與人員資料對照系統版113.2版第二項
- 新版115版第三大項 使用動物對照系統版113.2版第三項
- 新版115版第四大項 跨機構資訊對照系統版113.2版第五項
- 新版115版第五大項 實驗目的對照系統版113.2版第七項
- 新版115版第六大項 使用活體理由(3R描述)對照系統版113.2版第八之1/2/3項
- 新版115版第七大項 實驗設計內容說明對照系統版113.2版第八之4項
- 新版115版第八大項 重複實驗無對照
- 新版115版第九大項 環境豐富化政策對照系統版113.2版第九之4項
- 新版115版第十大項 非醫藥等級化合物(NPGC)對照系統版113.2版第九之5項
- 新版115版第十一項 麻醉/止痛/鎮靜使用對照系統版113.2版第九之3項
- 新版115版第十二項 疼痛/緊迫描述對照系統版113.2版第九之6項
- 新版115版第十三項 人道終點對照系統版113.2版第九之7項
- 新版115版第十四項 安樂死描述對照系統版113.2版第九之8-c項
- 新版115版第十五項 危害性物質使用對照系統版113.2版第十項
- 新版115版第十六項 參考文獻無對照
- 新版115版附錄一 繁殖計畫書對照系統版113.2版第四項
- 新版115版附錄二 手術計畫書對照系統版113.2版第九之3項
詳情請參照中心「實驗動物管理照護系統」公佈欄,農業部公告動物實驗計畫申請書(新案)改版,自115年2月1日起適用與本校新版動物實驗計畫書(115版)申請&審查方式之公告說明。